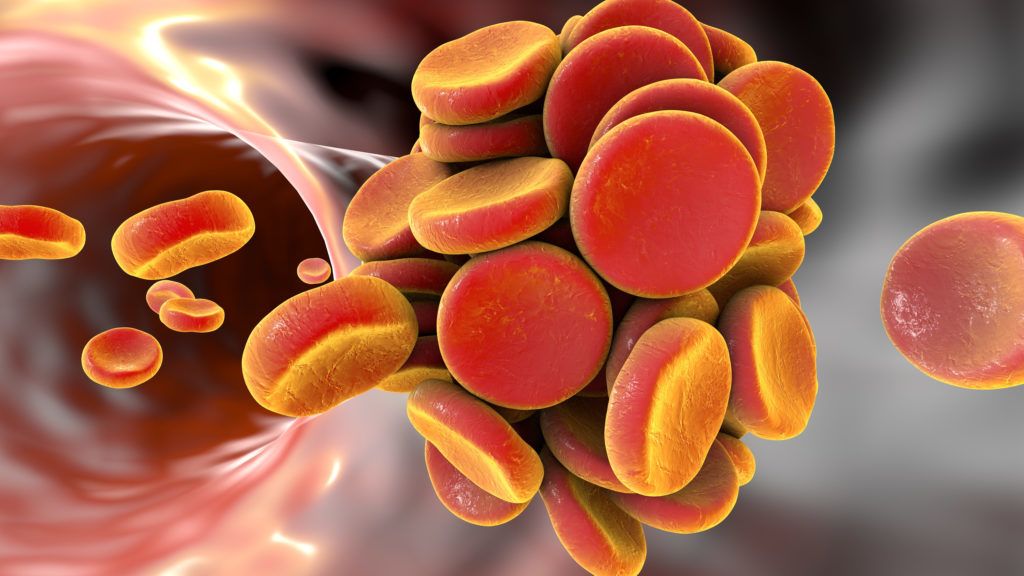
A véralvadás életmentő folyamat, ez biztosítja, hogy sérülés esetén ne veszítsünk túl sok vért. Az alvadás egyensúlya azonban időnként felborul, és a sérülés helyéről olyan helyekre kerülnek vérrögök, ahova nem kéne, illetve ezek akár sérülés nélkül is létrejöhetnek.
A gondokat okozó vérrögök természetéről és az eltávolítási lehetőségekről dr. Varjú Imrével, a Semmelweis Egyetem Orvosi Biokémiai Intézetének munkatársával, a Hemosztázis Kutató Részleg tagjával beszélgettünk annak kapcsán, hogy több másik kutatócsoport együttműködésével nemrégiben egy témába vágó tanulmányuk jelent meg a Nature Scientific Reports című lapban.
A VÉRALVADÁS LÉPÉSEI
Mielőtt rátérnénk arra, milyenek is azok a vérrögök, amelyek a szívroham vagy agyi sztrók hátterében állhatnak, és mit lehet tenni ellenük, nézzük meg, hogyan zajlik a véralvadás „normális” esetben.
A véralvadás az a folyamat, melynek során a vér szilárd halmazállapotúvá válik. Az alvadás lassítja le a vér elszökését a sérült érfalon át, és gátolja, hogy a seben keresztül kórokozók jussanak a vérbe.
Mindez egy rendkívül összetett folyamat eredménye, amelynek alaplépései a következők:
- amikor egy eret sérülés ér, annak falai először is összehúzódnak.
- Aktiválódnak a vérlemezkék (trombociták), amik egymáshoz és a sérült érfal kollagénrostjaihoz tapadnak, fizikailag eldugaszolva a sérülést.
- További elemek épülnek be a dugóba annak stabilizálása érdekében, és létrejön a véralvadék.
A vérlemezkékből álló kezdeti dugó nagyon gyenge, csak átmenetileg állja útját a vérzésnek, ezért a hálóba rendeződő lemezkék olyan anyagokat engednek szabadjára, amiktől megerősödhet a struktúra.
A több lépésből álló folyamat végén egy vérben állandóan jelen levő, nem aktív fehérjéből, a fibrinogénből fibrin keletkezik, amely erős hálót formál a sérülés felett. Ebbe a hálóba aztán újabb vérlemezkék, sejtek és más összetevők akadnak bele, tovább alakítva annak szerkezetét.
OLDÁS ÉS KÖTÉS
A szervezet számára persze nagyon fontos, hogy az így létrejött és stabil vérrög csak a sérülés helyén alakuljon ki, éppen ezért a véralvadással párhuzamosan egy másik folyamat is beindul.
Az ép érszakaszok sejtjei egy aktivátort kezdenek termelni, ami a plazminogén nevű előanyagot aktiválja. Amikor az aktivátor és a plazminogén összetalálkozik az alvadékon, egy enzim, a plazmin jön létre: ez képes széthasítani a fibrinhálót, felszabdalva azokat a vérrögöket,
Az egészséges szervezetben a két folyamat, tehát a véralvadás és az alvadék oldása tökéletes egyensúlyban van, vagyis csak ott maradnak meg az alvadékok, ahol sérülést dugaszolnak el, és a test többi részén ezek vagy ki sem alakulnak, vagy viszonylag gyorsan megsemmisülnek.
A problémák akkor kezdődnek, amikor az egyensúly felborul, és a véralvadás vagy a vérrögképződés akadályozása túlsúlyba kerül. Az első esetben vérrögök kerülnek ép érszakaszokba, elzárva ezeket, a másodikban pedig a vér nem alvad megfelelően, így minden apró sérülés erős vérzéssel járhat.
KÉNYES EGYENSÚLY
„Azt mindenki elvárja a szervezettől, hogy ha megvágom az ujjam, megalvadjon a vér, de azt senki sem szeretné, hogy máshol is megalvadjon” – mondja Varjú Imre, aki kollégáival először a Semmelweis Egyetemen, majd a Harvardon, Fulbright-ösztöndíjasként kutatta a folyamatot, jelenleg pedig a Columbia Egyetemen végzett egészségkommunikációs tanulmányai mellett vizsgálja a vérrögöket.
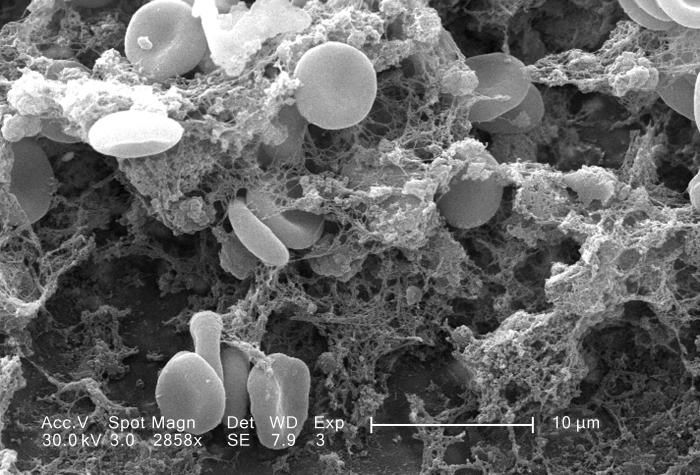
Az egyensúly biztosítását az alvadékot feloldó rendszer segíti: ahol nincs érsérülés, az alvadékot feloldó rendszer túlsúlyra jut az alvadékot létrehozó rendszerrel szemben, folytatja a szakértő.
Ha az egyensúly felborul, mert egy olyan masszív alvadási inger kerül az érpályán belülre, aminek ott nem lenne helye, azt nem tudja ellensúlyozni a rendszer. A leggyakrabban ez akkor történik, ha valakinek érelmeszesedése van, és az érfal alatt növekvő meszes-zsíros plakk addig növekszik, amíg egyszer csak beleomlik az érpályába”
– magyarázza Varjú Imre. A plakk tartalma által kiváltott erős alvadási ingerrel a szervezet egyedül nem képes megbirkózni, és az így a kialakuló vérrögök ép érszakaszokat zárhatnak el. Ami különösen problémás, ha olyan részeken akadnak meg, ahol nehezen hozzáférhetők.
A VÉRRÖGÖK SEM EGYFORMÁK
Mivel az erek elzáródása után az azok által ellátott szövetek gyorsan elkezdenek elhalni, a vérrögöt vagy fizikailag (infarktus esetén például katéterrel) kell eltávolítani, vagy ha ez nem járható út,
Agyi sztrók esetén ehhez jelenleg általában a szervezet saját módszerét másolják a szakértők, vagyis plazminogén-aktivátorokat juttatnak a testbe, hogy a létrejövő plazmin átvágja a fibrinhálót.
A vérrögök azonban nagyon sokfélék lehetnek, és ahogy az elmúlt évek kutatásai rávilágítottak, még messze nem tudunk mindent ezekről, márpedig hatékony és gyors oldásukhoz kulcsfontosságú, hogy tisztában legyünk összetételükkel és szerkezetükkel is.
A Semmelweis Egyetem Hemosztázis Kutatócsoportja Kolev Kraszimir professzor irányítása alatt pontosan ezzel foglalkozik, vagyis azt vizsgálják, milyen elemek kerülhetnek bele a vérrögökbe, és ezek hogyan befolyásolják a rögök fizikai és kémiai stabilitását.
A most megjelent cikkben, amit Farkas Veronika Judit és Varjú Imre közösen jegyez első szerzőként, a szakértők a vérlemezkék egyik komponensének szerepét vizsgálták a vérrögképződésben.
SOKOLDALÚ VÉRLEMEZKÉK
„Az, hogy a vérlemezkék befolyásolják a véralvadást, nem újdonság, hiszen nélkülük nem lenne alvadási folyamat. Az viszont talán kevésbé ismert, hogy az alvadék stabilizálásában is aktívan részt vesznek. A fibrinhálózathoz tapadt vérlemezkék ugyanis az idő múlásával egyre inkább elkezdik maguk felé húzni a hálót, és közben olyan komponensek szabadulnak fel belőlük, amik aztán közvetve szintén hozzájárulnak a véralvadék stabilitásához” – mondja Varjú Imre.
„Mi azt néztük meg, hogy ha a vérlemezkét lerakjuk egy felszínre, ahova oda tud tapadni, akkor milyen gyorsan terül ki ezen a felszínen. Ez fontos, hiszen a vérlemezkének a sérülés helyén szét kell terülnie, hogy minél nagyobb felszínt takarjon be. Azt láttuk, hogy ha kirakjuk egy felszínre és gátoljuk a CypD-t, akkor gyorsabban terül a vérlemezke” – magyarázza a szakértő.
Ez részben megmagyarázhatja a CypD-vel kapcsolatos ellentmondásos eredményeket, vagyis hogy miért tűnik úgy, hogy a fehérje gátlásával akadályozódhat, de növekedhet is a trombózis kialakulásának esélye. Egyrészt a fehérje hiánya a jelek szerint gyorsítja az alvadást, másrészt viszont
„Mindez két okból is fontos. Egyrészt már léteznek gyógyszerek (például egyes, a transzplantált betegekben használt immunrendszert gátló szerek) amelyek képesek a CypD gátlására. Ezek kapcsán nagyon lényeges megérteni, pontosan milyen (mellék)hatással bírnak a véralvadásra. Másrészt, amennyiben tisztázódik a CypD pontos szerepe a vérlemezkékben, az terápiás célpontként szerepelhet a véralvadási zavarok kezelésében” – mondja Varjú Imre.
SEJTSZINTŰ VADNYUGAT
A rögök a már említett összetevőkön (vérlemezkék, fibrinháló) túl más dolgokat is tartalmaznak, amik szintén komoly befolyással lehetnek arra, hogy mennyire lesz nehéz feloldani az alvadékot. Ilyen fontos tényezők a fehérvérsejtek is, amelyeket a Hemosztázis Kutatócsoport szintén vizsgál.
Másfél évtizede aztán kiderült, hogy egy rendkívül szervezett folyamat főszereplői. Gyulladás esetén ezekben a fehérvérsejtekben a maghártya eltűnik, és a sejtmag anyaga keveredik a sejtplazmával. Végeredményként egy fehérjékből és DNS-ből álló háló jön létre, amely a sejtmembrán felhasadásával lasszóként dobódik ki, hogy elfogja a kórokozót, mondja Varjú Imre.
Ezek a hálók, az ún. NET-ek akkor is létrejönnek, ha kórokozók nincsenek, de a gyulladási inger és a vérrögképződés beindult, mert például meszes-zsíros anyagok kerültek az érpályán belülre. És a NET-ek a fibrinhálóval összefogva kémiailag még stabilabb alvadékot hoznak létre, amit még nehezebb lesz oldani.
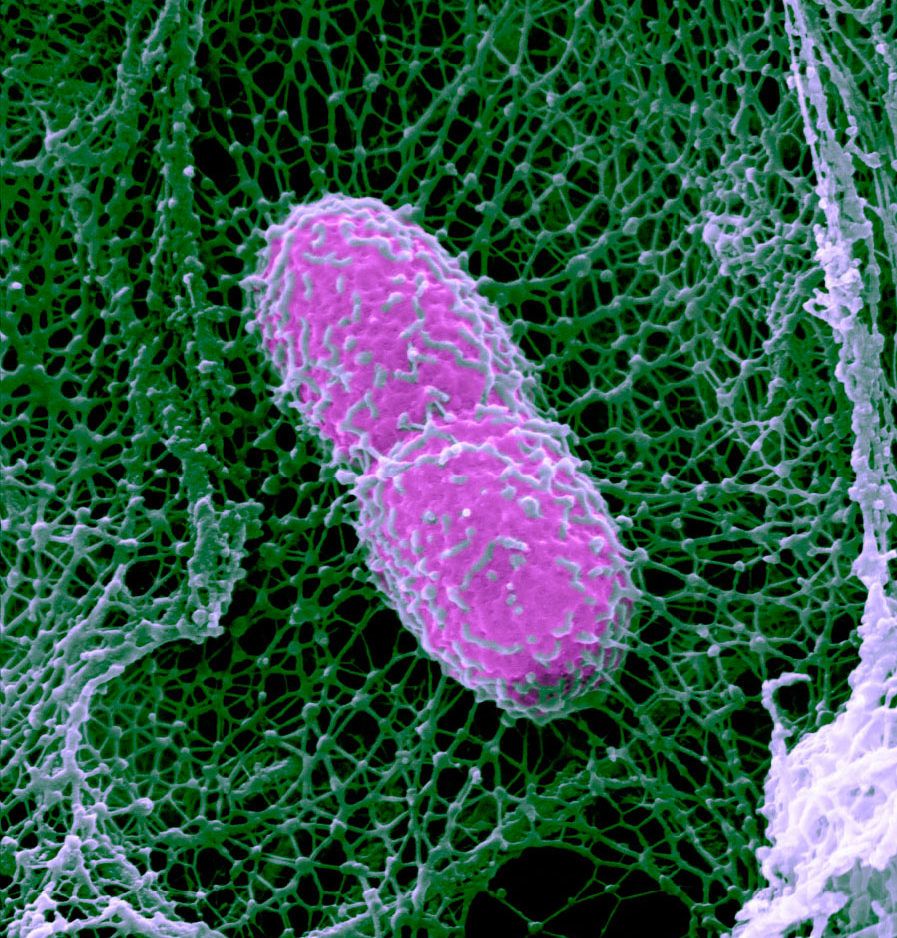
BAKTERIÁLIS FEGYVERTÁR
A kutatócsoport ezért azt is vizsgálja, hogy a NET-ek hogyan befolyásolják az alvadást, és a kialakuló vérrögök szerkezetét, illetve hogy mit lehetne ellenük bevetni a vérrögök oldása során.
Ennek kapcsán Varjú Imre elmondta, hogy a kutatásnak egy érdekes aspektusát jelentik bizonyos baktériumok, amik egyszerre termelnek a gyógyászatban a vérrögök oldására jelenleg is használt plazminogén-aktivátorokat és DNS-bontó enzimeket is.
Annak idején, amikor kiderült, hogy egyes kórokozók képesek a fibrinhálót vagdosni, ami használható lehet a vérrögök oldásában, óriási erőfeszítésekbe került, hogy az ezért felelős fehérjét izolálják a szakértők. Az ugyanis nagyon tapadt a DNS-t vagdosó fehérjéhez, amelyről mindenki azt hitte, hogy semmi haszna nincs, és le kell onnan pucolni, mondja a kutató.
A fibrinvágó fehérjét végül sikerült leválasztani, de most itt vagyunk évtizedekkel később, és kiderül, hogy mégsem kellett volna szétszedni a kettőt, mert nem véletlenül volt az úgy a baktériumokban sem”
– folytatja Varjú Imre. Ami a kutatócsoport jelenlegi munkáját illeti, a tagok elsősorban arra koncentrálnak, hogy a klinikai gyakorlatba ültessék át az eddig a vérrögökről megtudott információkat. Ehhez betegekből eltávolított vérrögöket vizsgálnak mikroszkóppal, és miután feltérképezték ezeket, megpróbálják az oldás szempontjából lényeges jellemzőket klinikai mutatókkal összepárosítani.
***
A Scientific Reports cikk szerzői: Varjú Imre, Farkas Veronika Judit, Kőhidai László, Szabó László, Farkas Ádám Zoltán, Polgár Lívia, Christos Chinopoulos és Kolev Kraszimir. A szerzők a Semmelweis Egyetem Orvosi Biokémiai Intézetében, a Genetikai, Sejt- és Immunbiológiai Intézetben, az MTA Anyag- és Környezetkémiai Intézetében, az MTA-SE Neurobiokémiai Kutatócsoportjában végezték kutatásokat, a tanulmány pedig az említett intézményeken túl a Harvard és a Columbia Egyetemeken íródott.
Kiemelt kép forrása: ThinkStock