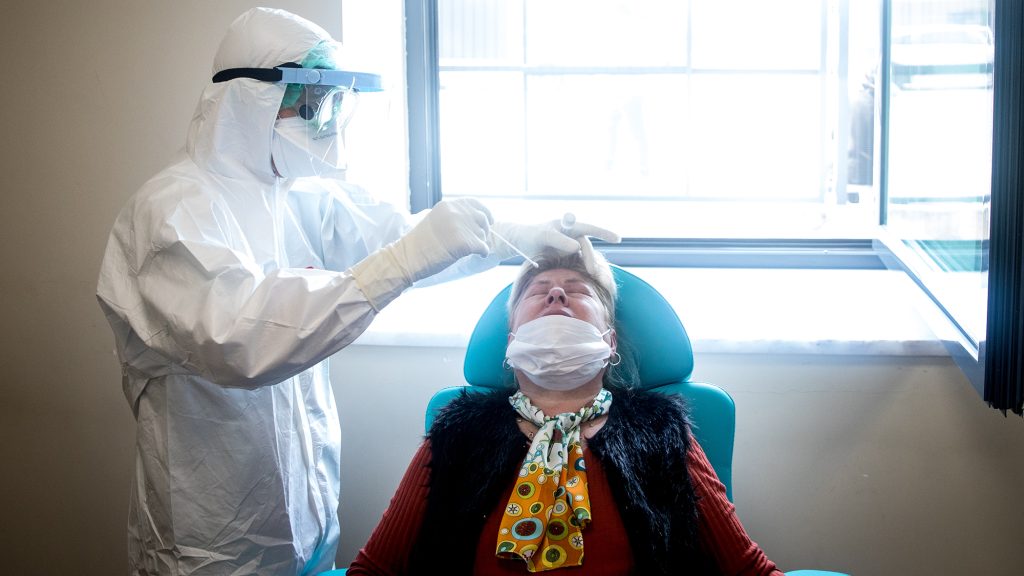
A koronavírus legújabb változatáról, az omikronról még mindig kevés, tudományosan megalapozott tudással rendelkezünk, ám annál több a feltételezés, a tévhit, a ténnyé formált remény. Ennek legfőbb oka, hogy a kutatási eredmények azonnal, kontextusukból kiragadva válnak hírré, a laikus pedig magára hagyva úgy értelmezi őket, ahogy tudja.
Dr. Falus András Széchenyi-díjas immunológust, akadémikust, a Semmelweis Egyetem professor emeritusát három olyan kérdéssel kerestük meg, amelyek talán fogódzót adhatnak az omikron világában.
- Mi az igazság az aktívabb megfertőződésről és az enyhébb betegségről?
- Ha enyhébb a betegség, az a posztcovid esélyét is csökkenti?
- Miért bicsaklott meg a vakcinák hatásossága?
Ellenanyagot gátló ellenanyagok
Sokakban motoszkálhat egy remény keltette feltételezés, miszerint az enyhébb betegség csökkentheti a posztcovid kialakulásának az esélyét. Bonyolult kérdés, hiszen maga a jelenség is új, alig ismert a tudomány előtt. „Definíció szerint” A panaszok rendkívül változatosak, rengeteg szervet érintenek, Falus professzor megfogalmazása szerint szinte a teljes belgyógyászati tankönyvet.
De mégis mi okozza, ha a vírusnak már nyoma sincs a testünkben? Biztosat nem tudunk. Létezik azonban egy hipotézis, ami az immunológiának egy ma még kevésbé ismert területére vezet – az 1970-es években fogalmazta meg Niels Jerne, Nobel-díjas dán immunológus. Azóta egyre gyűlnek a közvetlen és közvetett bizonyítékok, ám hangsúlyozzuk: pusztán egy elméletről van szó, amely ugyanakkor magyarázatot adhat a posztcovid jelenségére is.
Az idiotípus-anti-idiotípus hálózatról van szó, az egymással kölcsönhatásban lévő antitestek és sejtek komplex hálózatáról, amely serkentheti vagy gátolhatja az immunológiai aktivációt. Immunrendszerünk aktivációja ugyanis a gátlásra épül, az aktivitást is a gátlás megszüntetése jelenti. Elképzelhető, hogy a vírus megjelenése nagy mértékben feltolja az ellene keletkező specifikus ellenanyag szintjét, emiatt újabb ellenanyag (anti-ellenanyag) keletkezhet, majd ha ennek mennyisége is átlép egy határt, vele szemben is újabb ellenanyag (anti anti-ellenanyag) jön létre, és így tovább:
Mindegyik az eggyel előtte lévőt gátolja, amíg szükséges. Hosszabb távon a hálózat korlátozza magát, mint egy egyre csillapodó rezgőmozgás, egyre kisebb mennyiségű újabb antitest képződik
– mondja a 24.hu-nak Falus András.
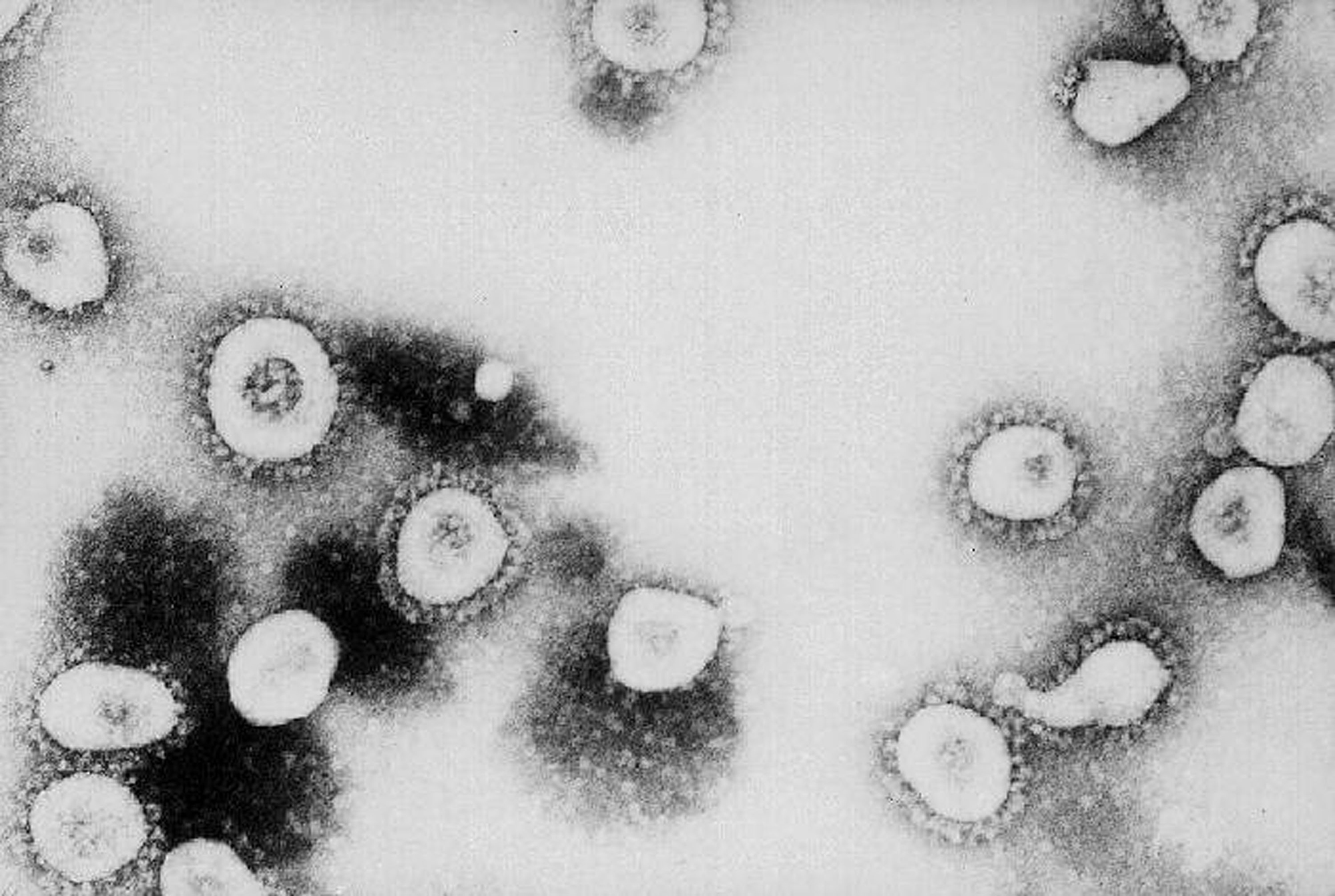
„Művírus” okozhatja a posztcovidot?
Hogy jön a képbe a posztcovid? Úgy, hogy a második ellenanyag, ami azon túl, hogy blokkolja az elsőt, olyan helyekre kötődhet, mint a vírus tüskefehérjéje, ezzel pedig immunválaszt válthat ki.
Képzeljük el, hogy egy kulcsot meleg viaszba nyomunk, ahol létrejön annak negatív lenyomata – a kulcs a koronavírus, a viasz az első ellenanyag. Ha a lenyomatba most megint viaszt öntünk, majd kivesszük, megkapjuk a kulcs pontos mását – ez a második ellenanyag, ami úgy néz ki, mint maga a vírus, ezért képes olyan helyekre kötődni, mint az eredeti kórokozó.
Létrejött egy »művírus«, amely reakciót vált ki, és a feltételezések szerint ez a »másolat« váltja ki a posztcovidot
– egyszerűsíti le a képletet a végletekig az immunológus professzor.
Más fertőzések, illetve egyes autoimmun betegségek után is ismert jelenség, hogy a tünetek a kórokozó jelenléte nélkül is visszatérhetnek. Jerne hipotézise szerint a fenti, idiotípus-anti-idiotípus elmélet lehet a magyarázat, amiről ismét hangsúlyozzuk: a közvetett bizonyítékok ellenére ma még tudományosan vitatott elképzelés.
A posztcovidhoz visszatérve tehát nem tudunk biztosat mondani, a válaszra váró kérdéseket felsorolni is túl hosszú lenne, ám a lényeg:
Szerencsés változás
A jó hír, hogy most már tényként kezelhetjük, miszerint az omikron okozta betegség az eddigiekhez képest enyhébb, mivel jelentősen csökkent a tüdő érintettsége. Mindezt viszont árnyalja a variáns elképesztően gyors terjedése: nagyon sok embert fog elérni, köztük olyanokat is, akiknek bármilyen okból is, de nagyobb a kitettségük.
Az omikron iszonyú sebességgel sokszorozódik, a szervezetbe jutott vírusmennyiség egy-másfél nap alatt a duplájára nő
– emeli ki Falus András.
A vírus számunkra szerencsés „újdonsága”, hogy úgy tűnik, elsősorban az orr és a száj nyálkahártyáit közelíti meg. Magyarán a felső légutakban koncentrálódik, ennek következményeként pedig nagyobb mennyiségben ürül, intenzívebben fertőz, de kevésbé jut el az alsó-légutakig, a tüdőbe.
A jelenlegi tapasztalatok alapján a fertőzöttek között sokkal kevesebb az elhunyt – ők is inkább egyéb betegségükből adódóan veszítik életüket, például a láztól –, és a kórházi ápolásra szorulók arányában is csökkenés várható. A nagy számok törvénye alapján viszont, mivel az omikron nagyobb tömeget ér el, nem biztos, hogy a kórházba kerülők száma csökkenni fog.
Megakadhat még a tüdő előtt
Az előző hullámokban megtanultuk az ACE2 kifejezést, ezekhez a receptorokhoz kötődik a sejteken a vírus tüskefehérjéje, vagyis rajtuk keresztül jut be a sejtbe. A tüdő sejtjei óriási mennyiségű ACE2 receptorral rendelkeznek, egyenes utat kínálva a vírus számára.
Az omikron ebben is más, és bár százszázalékos magyarázattal nem tudunk szolgálni, de az okot illetően van már egy erős hipotézis. E szerint az omikron más receptorokhoz, például egy úgynevezett CD147 fehérjereceptorhoz is aktívan kötődik, ez viszont a felső légutakban is nagyon szép számmal megtalálható.
Elképzelhető, hogy ezek a receptorok »megszűrik« a fertőzést, a vírus »elakad« bennük, mielőtt mélyebb régiókba jutna
– foglalja össze a lényeget a professzor.
Az omikron, mint egy módosult rakétafej
Ami a védőoltásokat illeti, a készítmények hatásossága kissé gyengébb az omikron ellenében, mint az eddigi variánsokkal szemben, de még így is lényeges védelmet nyújtanak – a legjobbat még mindig, illetve a gyártók folyamatosan „aktualizálják” a vakcináikat. A kérdés viszont, mi okozza a részleges vakcinaelkerülést.
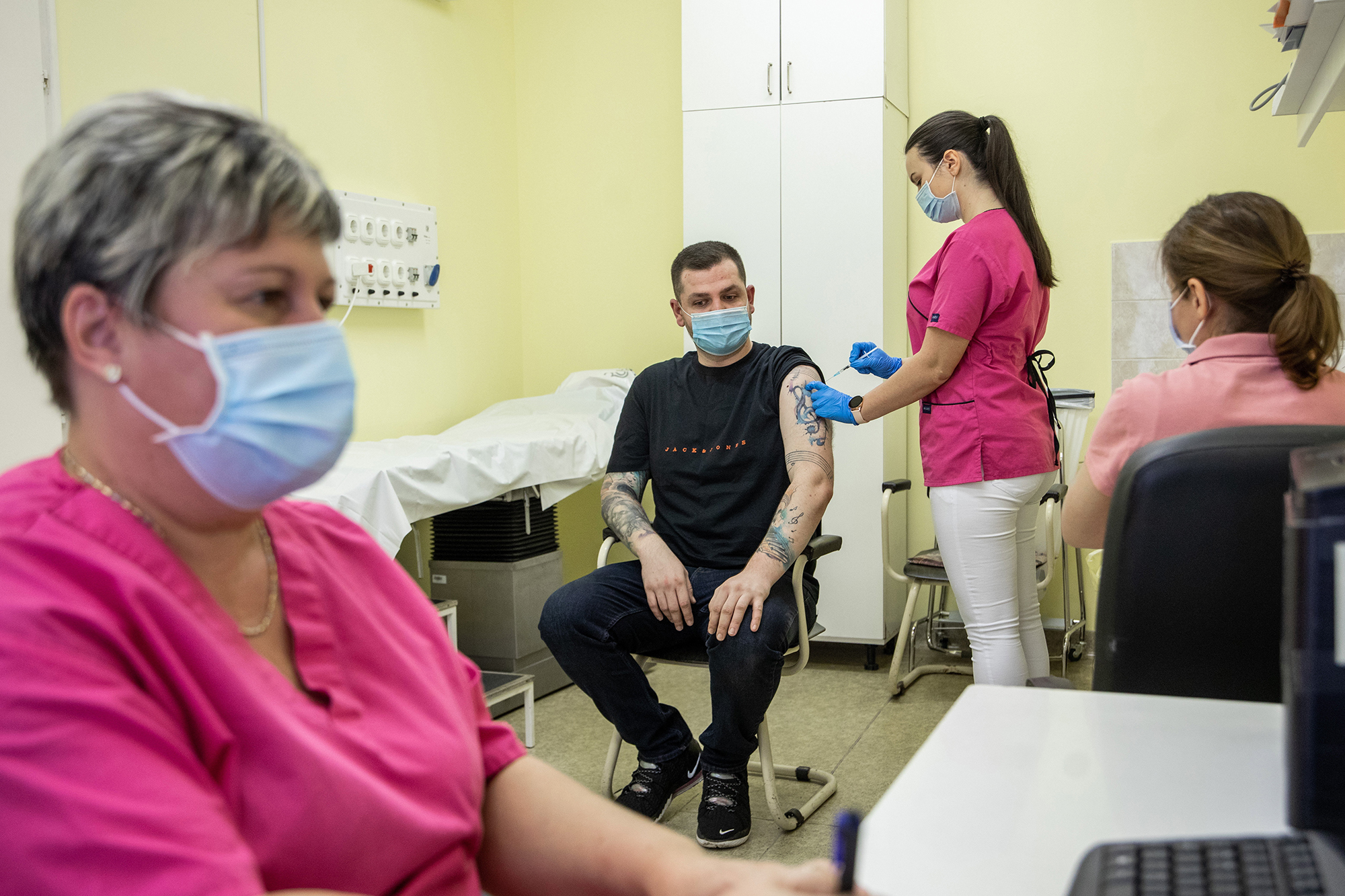
Képzeljük el úgy az omikron vírust, mint egy rakétát, amelynek speciális feje biztosítja, hogy áttörje a bunker tetejét, és odabent robbanjon. Ez a rakétafej esetünkben a tüskefehérje csúcsa, amely a már említett receptorokhoz illeszkedik. A vakcinák pedig – a kínai gyártmányú Sinopharmot kivéve – a tüskefehérjén keresztül váltják ki az immunválaszt, azaz biztosítják a szervezet védelmét.
Na most: maga a tüskefehérje viszonylag nagy, 1273 aminosavból áll, a csúcsa pedig, ami példánkban a rakéta speciális feje, 222 aminosavból épül fel, és RBD-nek nevezzük. Az immunizálás tehát a tüskefehérjére alakul ki, rengeteg céltábla van rajtuk, amelyeket az immunrendszer sejtjei felismernek – és hozzájuk kötődnek az ellenük termelt antitestek is azért, hogy elpusztítsák őket. Ezek a célpontok az úgynevezett epitópok.
Kitakarta a céltábláit
Egyes epitópokra ugyanakkor aktívabb immunválasz érkezik, másokra kevésbé aktív, előbbiket hívjuk immundomináns epitópoknak. Az omikron RBD felületén eddig soha nem látott számú, több mint 30 módosulás ment végbe. Olyan pontmutációk, amelyek befolyásolják céltábla (vagy célkereszt, célpont) jellegüket.
Az igazán protektív immunválasz mindig az RBD ellen irányul, így, ha a mutációk »kitakarják« a céltáblákat, csökken az immunitás aktivitása
– magyarázza Falus András, majd ismét kiemeli: a most alkalmazott, még az első variánsra fejlesztett oltások ezzel együtt is nagyfokú védelmet nyújtanak az omikron ellen.
Pár szó erejéig érdemes kitérni a teljes, elölt vírust alkalmazó kínai Sinopharm vakcinára. Laikusként gondolhatnánk, ez nemcsak a tüskefehérjére, hanem a teljes kórokozóra „megtanította” tüzelni a szervezetünket, így logikusan jobb találati arányt ér el.
Csakhogy ez ennél sokkal bonyolultabb, az egyszerű válasz pedig a nem: az Sinopharm eddig is gyengébbnek mutatkozó teljesítménye mit sem javul az omikronnal szemben. Rengeteg antigén ellen ad immunválaszt, a szervezet tényleg nagyon sok mindenre lő, de a most létrejött mutálódásokra nem.
Összességében tehát azt mondhatjuk, hogy az omikron okozta betegség nem annyira súlyos, de gyors terjedése veszélyeket rejt. A posztcovid szempontjából mindegy, hogy omikron, delta vagy bármi más okozta a fertőzést, a vakcináltság pedig egyéni és társadalmi szinten is elengedhetetlenül fontos.