A látást érintő betegségek nagyon nagy részéért a retina nem megfelelő működése felel, ritka az, ha az agyi érzékeléssel van probléma. A retinitis pigmentosa betegségcsoport mintegy 250 genetikai elváltozást takar, az összes látásvesztés nagyjából 10-20 százalékáért felelős. A génterápiák megjelenése előtt az ebben szenvedők gyakorlatilag tehetetlenül fogadták, hogy lassan elvesztik a látásukat – most azonban felcsillant a remény, hogy a látásromlásuk legalább egy bizonyos mértékig, ha nem is teljesen, visszafordítható lesz.
Roska Botond neurobiológus húsz évvel ezelőtt vetette fel először, hogy génterápiával gyógyítani lehet a genetikai elváltozások miatt kialakuló teljes vakságot. Ekkor azonban még nem volt meg a technológiai háttér ehhez, nem is csoda, hogy a kutatót évekig nem vették komolyan. A mára részletesen kidolgozott és a technológiai fejlődés révén lehetővé tett módszer első publikálása, 2008 óta figyelt fel a tudományos szakma is a génterápiás látásjavításra, most pedig ott tartunk, hogy hétfőn, az első klinikai kísérletből készült tanulmány publikálásával új tudomány született: a vizuális rehabilitáció, ami 13 éves munka eredménye.
„Egy amerikai kérdőíves kutatás során kiderült: az emberek a vakságot a legrosszabb egészségügyi problémának tartják” – mondta el Roska Botond egy online sajtótájékoztatón. „Szorosan mögötte van az Alzheimer-kór és a daganatos betegségek. Ez nemcsak azért lehet így, mert a biológiánk látásközpontú, hanem azért is, mert az olyan eszközök nélkül, mint az okostelefon és a laptop, nagyon sokan még dolgozni sem tudnának.”
A látás hamburgere
A látás egy nagyon bonyolult folyamat. Úgymond egy videóval kezdődik, amit a szemünk, vagyis a szem hátulján található fényérzékeny réteg, a retina veszi fel. „A retina tulajdonképpen egy biológiai számítógép, a beérkező videónak nagyjából 30 reprezentációját hozza létre. Az agyunk nem lát, ez csak ezekből a videókból próbálja megjósolni a valóságot.” A retina által készített „videók” először az agy központjáig, majd a látókéregig jutnak, a vizuális információ pedig gyakorlatilag behálózza az egész agykérget.

Roska Botond egy hamburgerhez hasonlította a látásban részt vevő mechanizmusokat az egyszerűbb érthetőség kedvéért: a hamburgerbuci felső fele a fényérzékeny réteg, a benne található hús és zöldségek a számítási rétegek, vagyis az a terület, ahol a látási kép létrejön, az alsó buci pedig a ganglionsejt réteg. A teljes vakság gyógyításához jelenleg négyféle különböző optogenetikai terápia létezik, ezek mindegyike a hamburger más és más rétegét érinti. Amiről a tanulmány szól jelenleg, az a ganglionsejteket érinti, de lehet terápiát alkalmazni a csapokra, a bipoláris sejtekre és az amakrin sejtekre is.
A retinitis pigmentosa esetében általában a hamburgernek nincs teteje, azaz nincs fényérzékelés egyáltalán nincs, vagy csak nagyon minimálisan. Az utóbbi volt a helyzet a tanulmányban bemutatott férfinél:
Számára a ganglionsejteket érintő terápiát alkalmaztak, azaz egyszeri injekciót kapott az egyik szemébe, amelyben úgynevezett adeno-asszociált vírusok vitték a megfelelő helyre azt a gént, ami egy különleges fehérje kódolásáért felelős. A csatornarodopszin vagy channelrhodopszin olyan fehérje, amely borostyánszínű fényt érzékel, ez biztonságosabb a retinasejtek számára, mint a toxikus kék fény. Az adeno-asszociált vírusoknak csak a nevük hasonlít a koronavírus-vakcinák némelyikében is használt adenovírusokra, valójában egy azoknál ötször kisebb, 20 nanométeres átmérőjű vírusokról van szó, amelyek magukban képtelenek a szaporodásra és a fertőzésre is, csak a postás szerepét töltik be az injekcióban.
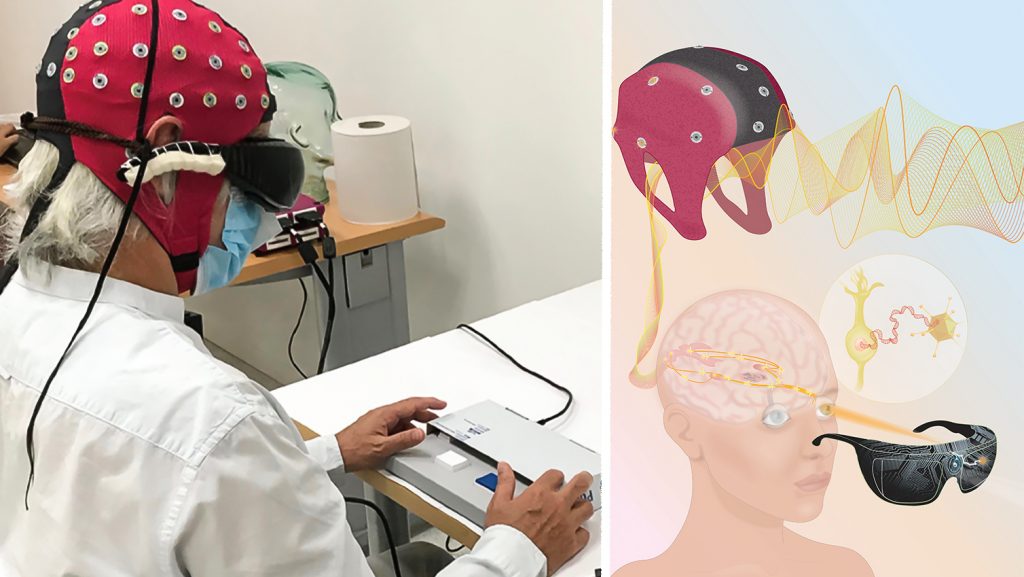
A kísérleti alany megkapta a vakcinát, majd otthon négy és fél hónapos tanulási idő következett: meg kellett ugyanis ismernie azt a szerkezetet, amit a génterápia után használnia kellett. A terápia magában nem elég, kell hozzá egy szemüveg, ami gyakorlatilag videót készít a szem számára, és azt vetíti a retinára, kiváltva a „számítási mechanizmusok” jó részét – így a munka oroszlánrészét átveszi ettől a biológiai számítógéptől, és a videót levetíti a ganglionsejteknek. A férfi több mint négy hónapig tanulta a szemüveg és a hozzá tartozó apró, zsebben hordható számítógép működését, majd amikor az utcán sétálva képes volt kivenni a gyalogátkelő felfestését, ez után kezdődtek el a kísérletek.

Fontos érteni, hogy ez nem ugyanaz a módszer, mint amit a saját szemünk használ. Mivel a férfi fokozatosan veszítette el a látását, vissza tudta idézni, milyen egy zebra felfestése, de a szemének és az agyának meg kellett értenie az új szignálokat. „A szem gyakorlatilag új nyelvet beszél, amit meg kell tanulnia a betegnek” – mondta Roska Botond.
A kísérletek során a férfinak először egy jegyzetfüzetet, majd egy kis dobozt, végül egy szinte teljesen átlátszó objektumot mutattak. A szemüveg segítségével sikerült látnia mindhármat, sőt amikor két poharat mutattak neki, meg tudta állapítani azt is, hogy egymáshoz viszonyítva hol helyezkednek el az asztalon. A beteg arról beszélt, hogy „egyfajta vertikális vibrációt” érzékelt. A látás nem színes, hanem fekete-fehér ilyenkor, és számít az adott objektum nagysága és kontrasztja is. Mivel biztonsági okokból csak egy szemet kezeltek a génterápiával, minél kevésbé akarták belekeverni a kutatók a három dimenziót belekeverni a kísérletbe, hiszen a térérzékeléshez szükség van mindkét szemre.
Egytől százas skálán azt mondanám, hogy ez egy tízes szintű látásjavulás, de ez csak az első lépés
– mondta a kutató. Fontos, hogy a vizuális kéreg is aktivitást mutatott a kísérleti alanynál, ebből az aktivitásból pedig számításokkal ugyanazt a képet tudták visszafejteni a szakértők, mint amit az alany látott.
A legegyszerűbb, de nem a legjobb módszer
Roska Botond megjegyezte, hogy ez ugyan a legegyszerűbb terápia a négy különböző lehetséges kezelés közül, de nem a leghatékonyabb: a „hamburgerben” minél feljebb kerülünk, és minél többet dolgozik maga a retina, annál jobb lehet az eredmény. Ennek azonban hátránya is van: a felső bucihoz közeledve fokozatosan kevesebb emberre lesz megfelelő az adott terápia. A ganglionsejtes terápia ugyanis nem tesz különbséget a vakságot okozó genetikai mutációk között, a többi viszont már egyre inkább.
Az első kísérleti alany látása valószínűleg még javul majd, a többi között abban kell még fejlődni, hogy minél kevesebb időre legyen szüksége a tárgyak felismeréséhez. Egy egészséges látással rendelkező ember szeme és agya ezt valós időben végzi, de a férfinek jelenleg még időre van hozzá szüksége. Szükség lehet még a ganglionsejtekre vetített videó módosítására a legjobb eredmény érdekében, és arra is, hogy a másik három terápiát eljuttassák az emberi kísérletekig. Ha pedig sikerülne a látható fényen túl jutni, és például infravörös fényt használni a borostyánszínű helyett, a pácienscsoport akár ezerszeresére is nőhetne, hiszen a nem teljes vakságot is képesek lennének gyógyítani. „Nálunk úgy folyik a munka, hogy állandóan hibázunk, de soha nem adjuk fel” – mondta a kutató. „Jelenleg a teljes vaksággal tudunk dolgozni, ott, ahol a látóideg még megvan, mert ha nem ez a helyzet, ahhoz már agyműtétre lehet szükség.”
„Én elsősorban kutató vagyok, nem én választom ki az önkénteseket a kísérletekhez” – jegyezte meg, kiemelve, hogy a Semmelweis Egyetemen már zajlik a pácienscsoportok összegyűjtése, ami elengedhetetlen ahhoz, hogy azok a cégek, amelyek klinikai kísérleteket végeznek, itt is találjanak megfelelő, jól karakterizált alanyokat.