Jelenleg a család négy gyermeke közül az ikerpárnál, Jennie-nél és James-nél fedezték fel, hogy a hibás gén, ami édesanyjuk halálát okozta, bennük is megvan. Mindkét testvérnél a nyakukban lévő vitális erek és idegek köré fonódó műthetetlen daganatokat találtak – írja az ELTE Diagnosztika és Terápia Kiválósági Program weboldala.
Azon túl, hogy a hibás gén működése gyakran vezet áttétek kialakulásához, a daganatok sok esetben önmagukban is műthetetlenek anatómiai elhelyezkedésük miatt. Ha mégis lehetségessé válna a beavatkozás, akkor maga a műtét jelentene veszélyt, mivel egy rutinszerű érzéstelenítés is végzetes lehet e ritka, daganatos betegségben szenvedőknél.
Az angol családban az úgynevezett pheochromocytomák (PHEO) ritka, örökletes neuroendokrin tumorok okozzák az idő előtti elhalálozást. Ezek a mellékvese velőállományából kiinduló tumorok túlzott adrenalin-szerű hormonokat pulzálnak a keringésbe. A PHEO-t nehéz diagnosztizálni, mert más betegségeket, például magas vérnyomást utánozhat, így felismeréséig sok idő telhet el. Sokszor csak utólag, a váratlan elhalálozás körülményeit vizsgálva derül ki, hogy a beteg a ritka, neuroendokrin daganattal küzdött.
Nemzetközi kutatócsoport és az áttörés
„Dr. Anil Mehtával, a Dundee-i Egyetem kutatójával tizenhárom éve foglalkozunk tumorgenetikával. Az azóta már a családról elnevezett Williamson-mutáció kutatásának története úgy kezdődött, hogy a Williamson család Anil szomszédja Skóciában, Dundee-ban.
A családfő felkereste Anilt, aki pedig nekem mesélt a tumor biológiai hátteréről – mondta Vellainé Takács Krisztina, a magyar kutatócsoport vezetője, az ELTE-n működő Diagnosztika és Terápia Kiválósági Program kutatója. „A Williamson-mutáció a szukcinát-dehidrogenáz (SDH) enzim B alegységét érinti. A B alegység hibája gyakran vezet daganatos áttétek kialakulásához, aminek a mechanizmusa jelenleg még nem ismert. Mivel az egér és patkány ennél a ritka tumornál nem bizonyultak jó modellszervezeteknek Dr. Aamir Nazirhoz fordultunk, aki az indiai Központi Gyógyszeripari Kutatóintézet kutatója, és neurodegeneratív betegségeket modellez fonálférgek (Caenorhabditis elegans) felhasználásával.”
A nemzetközi kutatócsoport közös munkája és a család együttműködése meghozta a remélt áttörést. „Az indiai és magyar egyetemek kutatóival közösen először tudtuk előállítani a Williamson-mutációt egy apró, mindössze egy milliméter hosszúságú féregben. Ez a felfedezés elengedhetetlen a káros hatások mechanizmusának megértéséhez, és segíthet rámutatni a rák lehetséges kezelésére” – mondta Dr. Anil Mehta.
A Williamson féreg a PHEO kísérleti patkánya
A Williamson család hibás génje, az emberi szervezet energiatermelésében szerepet játszó, egyik fontos fehérjéjének, az úgynevezett SDHB fehérje szerkezetét változtatja meg. Az SDHB-fehérje funkciója a tudományos-fantasztikus irodalomból vett példával élve hasonlít a Vissza a jövőbe című filmekben Doki időutazó DeLorean sportkocsiját hajtó, vízzel működő „fluxuskondenzátorhoz”, ami a vízből hatalmas energiát képes előállítani.
A biológiában az SDHB fontos eleme, az emberi fluxuskondenzátornak, vagyis annak a folyamatnak, ami az elfogyasztott tápanyagból energiát állít elő.
„A DNS genetikai manipulációjával nemzetközi csoportunk létrehozta az SDHB-gén meghibásodásának féregmodelljét. Azért választottunk férgeket a PHEO modellezéséhez, mert a férgek SDHB génje több százezer év alatt lényegében változatlan maradt. Az állati sejtekben általánosan működő energiagenerátor több mint 400 millió évvel ezelőtt tökéletesedett, és változatlanul működik ma is” – mondta Vellainé Takács Krisztina.
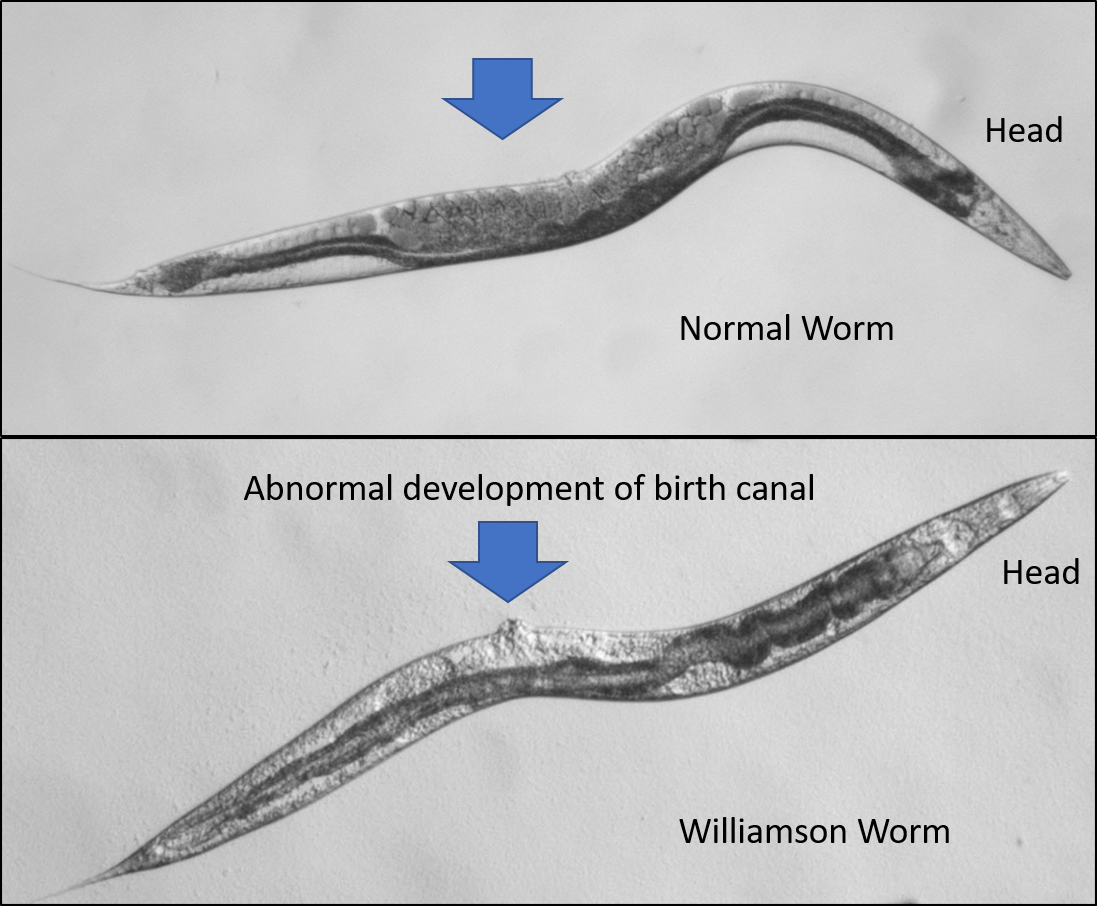
Reménykeltő eredmények
Az új modellállat egyértelmű siker. A férgekben megjelent a Williamson-mutáció, ami további, pontosabb vizsgálatok tesz lehetővé. Sikerült a kutatóknak szelektíven kezelni a Williamson mutáns férgeket úgy, hogy közben az egészséges férgek életben maradtak. Ez azt jelenti, hogy bizonyos hatóanyagok a Williamson férgeket elpusztítják, míg az egészséges állatokra nincsenek hatással. Vagyis a humán rákos sejtek ellen is lehetnek megfelelő hatóanyagok, amik teszteléséhez egy lépéssel közelebb kerültek a kutatók. Jelenleg nincs gyógymód a PHEO-tumorok ellen, de a kutatások eddigi eredményei új utakat nyithatnak a daganatos megbetegedéssel kapcsolatos vizsgálatokban és a tünetek felismerésében.